Så funkar solceller
Det snackas mycket om solceller och solpaneler. Men hur fungerar de egentligen? Här gör vi ett försök att förklara principen. Vi börjar med en gammal dansk.
Dansk upptäckt lade grunden
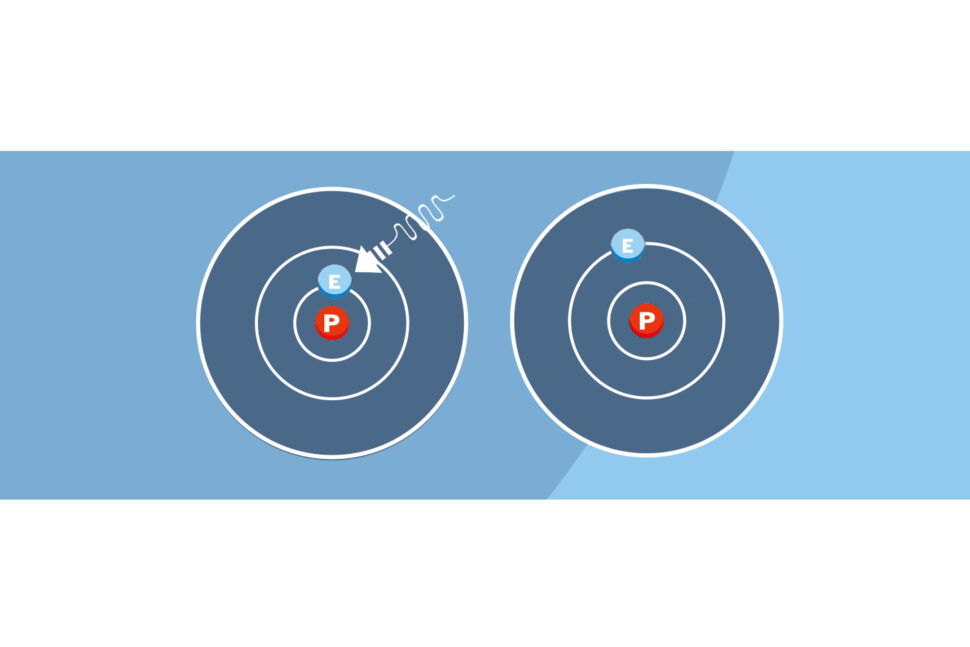
Danske fysikern Niels Bohr föreslog 1913 den modell av väteatomen som förklarar principen för hur en solcell kan generera elektrisk spänning. Han fastslog att ljus kunde påverka vätemolekylens enda elektron. Det Bohr fann var att om en ljuspartikel – en ’foton’ – träffar väteatomens elektron så absorberar den fotonens energi och flyttar ut till en elektronbana som ligger på längre avstånd från kärnan. Att elektronen flyttat sig beror på att den fått en högre elektrisk laddning än tidigare. Varje elektronbana kräver sin egen förutbestämda laddning som matchar den attraherande kraften från atomkärnan. Om elektronen sedan skulle flytta tillbaka till en lägre bana kommer den att istället avge sin överskottsenergi – i form av en foton.
Tre ämnen med olika egenskaper
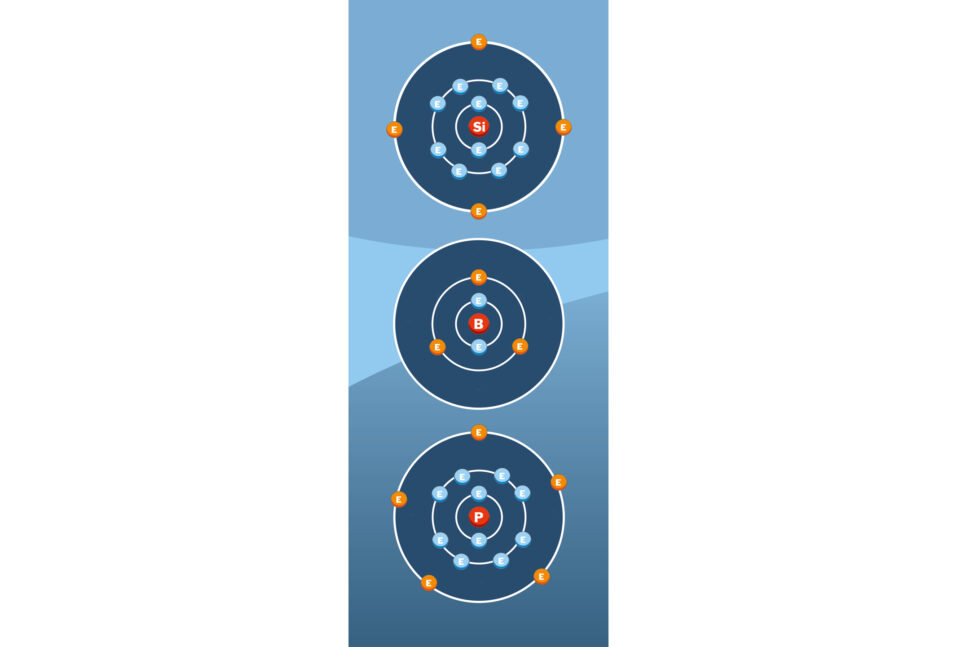
I en solcell av den typ som är vanligast idag är det egenskaperna hos tre olika grundämnen som utnyttjas. Det som skiljer dessa ämnen åt är hur många elektroner de har i sin yttersta elektronbana. Sådana elektroner kallas ’valenselektroner’ och de har en viktig egenskap i det här sammanhanget: När två atomer förs närmare varandra attraheras valenselektronerna i de respektive atomerna av kärnan i den andra. Parvis kommer de att delas av båda atomerna och skapar då vad fysikerna kallar en ’kovalent molekylär bindning’. Den översta atomen här är en kiselatom. Kisel, Si, är det viktigaste ämnet i solcellen, det ämne som den egentligen är uppbyggd utav. Kisel har fjorton protoner och fjorton elektroner, med fyra valenselektroner i den yttersta banan. De fyra valenselektronerna binder samman en kiselatom med fyra andra och bildar på så vis en kiselkristall – den pyramidformade juvelen inom modern elektronik.
I solcellens övre skikt är kiselatomerna ’dopade’ med grundämnet bor (B) för att kislets egenskaper ska ändras. Boratomen, i mitten, har bara fem elektroner, varav tre är valenselektroner. När bor binder till kisel uppstår en ofullständig bindning som kan dra till sig en fri valenselektron i närheten. Denna elektron lämnar efter sig ett ’hål’ som kan röra sig fritt i kristallen. Boratomen bildar ett negativt område i kristallen. Kiselkristaller som dopas med bor sägs vara ’P-dopade’.
I det nedre skiktet i cellen är kiselatomerna dopade med fosfor (P). Fosfor har gott om elektroner – 13 stycken. Fem av dem är valenselektroner. I bindningen med kisel blir en av dessa elektroner över och kan röra sig fritt. Eftersom fosfor har en proton mer än kisel får fosforatomen en positiv laddning i kristallen. När kiselkristallen dopats med en fosforatom säger man att kislet är ’N-dopat’.
PN-övergången
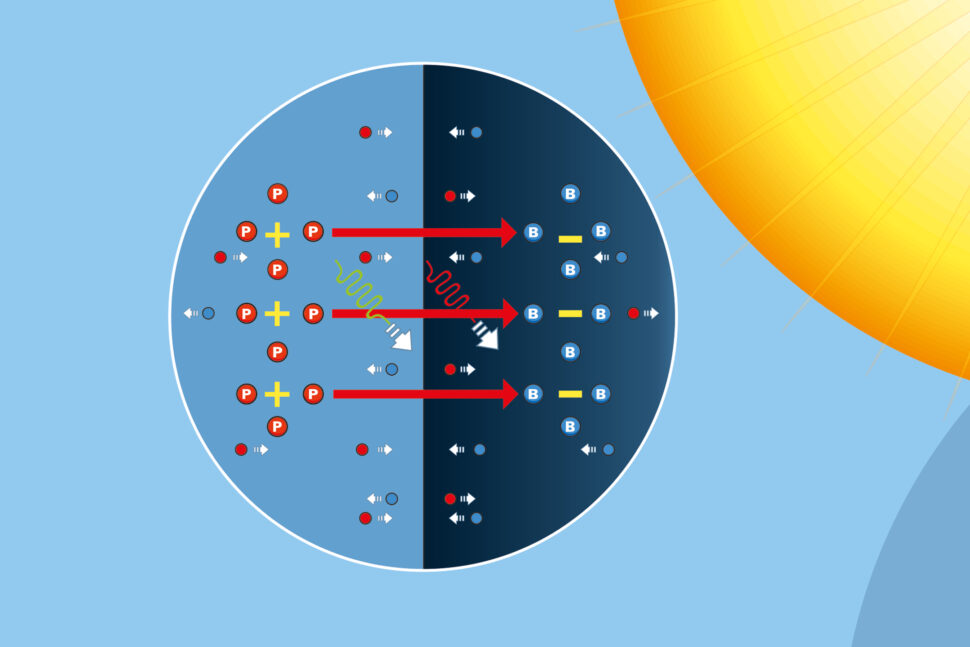
Om man fogar ihop en N-dopad och en P-dopad halvledare – i vårt fall kisel – till en enda kristall kommer elektroner från N-delen vandra till P-delen och fylla de positiva hålen där. Likadant kommer hål från P-delen vandra över till N-delen och där ’ta upp’ elektroner. Den elektriska laddningen i kristallen neutraliseras inte längre av ledningselektronerna eller hålen utan kristallen får två skikt med olika laddning.
Vandringen av hål från P-området och elektroner från N-området kommer att fortsätta tills det elektriska fältet skapat en spänningsbarriär som laddningarna inte kan passera. När en sådan ’PN-övergång’ väl har bildats får den egenskapen att den leder ström mycket bättre i ena riktningen än i den andra. Ansluter man då en spänningskällas positiva pol till P-delen och den negativa polen till N-delen, kommer spänningsbarriären att sänkas och ström kommer att flyta genom kretsen. Om man sen sätter ut halvledaren i solen kommer fotoner att slå loss elektroner som i sin tur lämnar efter sig positivt laddade hål. Elektronerna och hålen kommer att vandra över till sina respektive sidor och på så sätt uppehålla spänningen och antalet ledningselektroner.
Miraklet ett faktum
Den kiselbaserade solcellen är uppbyggd i fyra olika skikt. Överst ett tunt skikt som fungerar som skydd för alla underliggande och som med sin mörka färg ökar absorptionen av ljus. Det skiktet är försett med tunna elektroder som sammanbinds i en kopplingspunkt.
Nästa skikt är det fosfordopade kiselskiktet, där själva PN-övergången finns. Under det fosfordopade skiktet finns ett tjockare bordopat skikt med underskott på elektroner. Nederst ett kontaktskikt som också samlar ihop elektrisk laddning i en kopplingspunkt.
När fotoner träffar det fosfordopade skiktet börjar elektroner röra sig ner till det bordopade. De negativt laddade hålen rör sig uppåt till borskiktet. Tack vare PN-kopplingen kvarstår spänningen i cellen så att den kan matas från det undre skiktet tillbaka till det övre – via en last, som i det här fallet symboliseras av en glödlampa. Lampan lyser!
Nyhetsbrev
Prenumerera på vårt nyhetsbrev och få nyheter, tips och bevakningar rakt ner i inkorgen